Sisu
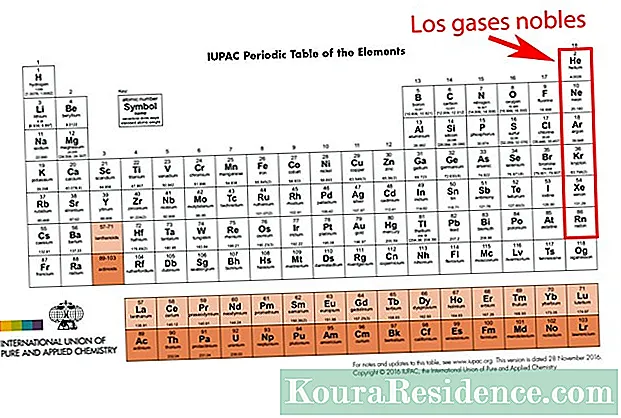
TheVäärisgaasid Need on keemiliste elementide kogum, millel on teatud omaduste vahemik, näiteks tavalistes tingimustes monatoomiline, lõhnatu ja värvitu, neid ei saa külmutada, nende keemistemperatuurid on väga kõrged ja neid saab vedeldada ainult suure rõhu all.
Eriti väärisgaaside sisaldus on väga madal keemiline reaktsioonivõime, see tähendab, et vähe kombineeritavust perioodilise tabeli muude elementidega. Sel põhjusel on nad saanud ka nime inertsed gaasid või haruldased gaasid, ehkki mõlemat nimetust tänapäeval ei soovitata.
See tähendab, et nendest gaasidest pärinevaid aineid on vähe, kuid mitte vähe. tööstuslikuks otstarbeks ja tavad:
Näiteks asendab heelium õhupallides ja õhulaevades vesinikku, kuna see on palju vähem tuleohtlik gaas; krüogeensetes protsessides kasutatakse vedelat heeliumi ja neooni. Argooni kasutatakse ka hõõglampide täiteainena, kasutades ära selle vähest tuleohtlikkust ja muid valgustusmehhanisme.
- Vaata ka: Ideaalse gaasi ja reaalse gaasi näited
Näited väärisgaasidest
Väärisgaase on ainult seitse, seega võib olla ainult neid konkreetseid näiteid:
Heelium (ta). Universumi suuruselt teine element, kuna tähtede tuumareaktsioonid tekitavad selle vesiniku sulandumisel, on see tuntud oma omaduste poolest, mis muudavad inimese häält sissehingamisel, kuna heli levib palju rohkem kiiresti läbi heeliumi kui õhu. See on õhust palju kergem, nii et see kipub alati tõusma ja seda kasutatakse sageli dekoratiivsete õhupallide täidisena.
Argoon (Ar). Seda elementi kasutatakse laialdaselt aastal tööstuses isoleeriva või inhibiitorina töötavate väga reaktiivsete materjalide tootmiseks. Nagu neoon ja heelium, kasutatakse seda ka teatud tüüpi laserite saamiseks ja tööstuses pooljuhid.
Krüpton (kr). Hoolimata inertsest gaasist, on teada reaktsioone fluoriga ning klatraatide moodustumisel veega ja muuga aineid, kuna sellel on teatud elektronegatiivsuse väärtus. See on üks elemente, mis tekivad ühendi lõhustumisel aatom uraani, seega on seal kuus stabiilset ja seitseteist radioaktiivset isotoopi.
Neoon (ne). Ka tuntud universumis on see element väga rohke, andes luminofoorlampide valgusele punaka tooni. Seda kasutati neoontorude valgustuses ja seetõttu pani ta sellele oma nime (hoolimata asjaolust, et teiste värvide jaoks kasutatakse erinevaid gaase). See on ka osa teletorudes leiduvatest gaasidest.
Ksenoon (Xe). Esimene raske gaas, mida leidus vaid jälgedena maakera pinnal, oli esimene sünteetiline väärisgaas. Seda kasutatakse lampide ja valgustite (näiteks filmides või autode esilaternates), samuti teatud laserite valmistamisel ja üldanesteetikumina, nagu krüptoon.
Radoon (Rn). Selliste elementide nagu raadium või aktiinium (sel juhul on see tuntud kui Actinon) lagunemise produkt, see on radioaktiivne inertgaas, mille stabiilseima versiooni poolväärtusaeg on enne polooniumi saamist 3,8 päeva. See on ohtlik element ja selle kasutamine on piiratud, kuna see on väga kantserogeenne.
Oganeson (Og). Tuntud ka kui eka-radoon, ununoktium (Uuo) või element 118: ajutised nimed hiljuti Oganesoni nimelise tranaktiniidse elemendi jaoks. See element on väga radioaktiivne, mille hiljutine uuring on sunnitud teoreetiliselt spekuleerima, mille põhjal on kahtlust, et tegemist on väärisgaasiga, hoolimata sellest, et see kuulub perioodilisustabeli 18. rühma. See avastati 2002. aastal.
- Gaasilise oleku näited
- Keemiliste elementide näited
- Gaasisegude näited